目次(移動できます)
ウイルスの構造
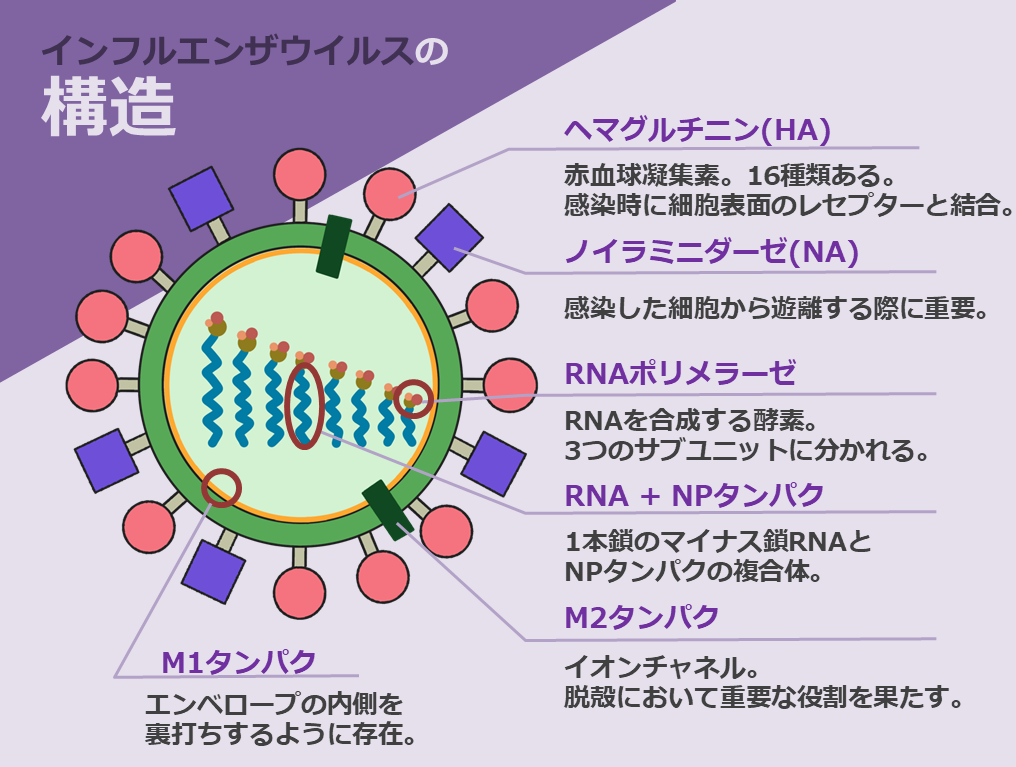
インフルエンザウイルスはオルトミクソウイルス科に属し、大きさは80-120ナノメートル(ナノは10億分の1)程度です。
上の図に示すように様々なタンパク質が含まれています。
脂質2重層からなるエンベロープ表面には赤血球凝集であるヘマグルチニン(HA)とノイラミニダーゼ(NA)が突出しています。
HAとNAはスパイクタンパク質と呼ばれ、ウイルスが増殖する際に細胞に吸着する段階で重要な役割を担います。
HAは最も多く含まれるタンパク質で40%を占めます。
NAはウイルスが増殖し終えた後に、細胞から遊離する際に不可欠です。
インフルエンザウイルスの遺伝情報は8本の(-)ssRNA(1本鎖のマイナス鎖RNA)が保持しています。
遺伝子はそれぞれNPタンパクに巻き付いて存在しており、一方の端には「PA」、「PB1」、「PB2」の3つのサブユニットからなるRNAポリメラーゼが結合しています。
M1タンパクはエンベロープ(ウイルスの外殻)を裏打ちするように存在し、実質的な殻の役割を持つとされています。
M2タンパクはウイルスのエンベロープを貫通するように存在します。
これはイオンチャネル型の膜タンパクで水素イオンを選択的に通過させる働きを持ちます。
このタンパク質のおかげでウイルス内部が酸性となり、RNAとNPタンパク複合体とM1タンパク質の結合とエンベロープの主要成分であるM1タンパク質自体の結合も弱められて、ウイルス遺伝子が感染細胞内に放出されます(脱殻)。
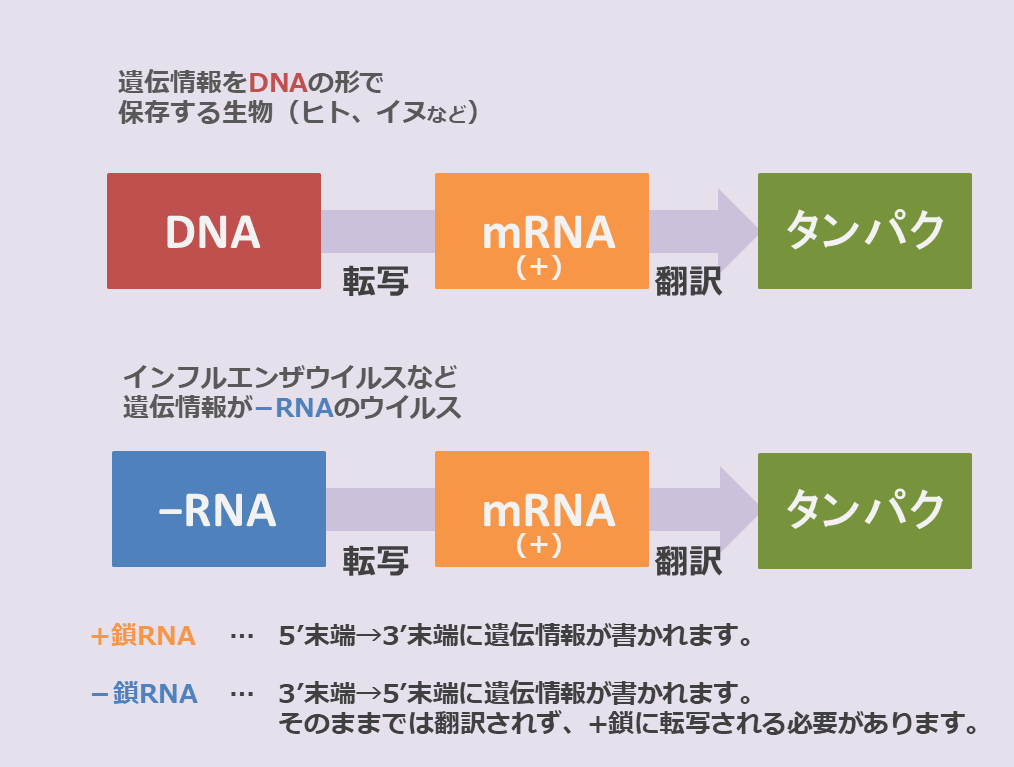
マイナス鎖RNAとは?
mRNA(メッセンジャーRNA)と同じように5’末端→3’末端方向に遺伝情報が書かれているのが「プラス鎖」と呼ばれるのに対して、逆に3’末端→5’末端方向に書かれているものが「マイナス鎖」です。
そのため、マイナス鎖は一度転写されてプラス鎖にならないとmRNAとして機能しません。
インフルエンザウイルスや麻疹ウイルスなどのマイナス鎖を持つウイルスは、RNAポリメラーゼを必ず内部に持っています。
ウイルスの特徴と感染する動物
インフルエンザウイルスには以下のような特徴があります。
①ウイルスに含まれるタンパク質の特徴によってA型、B型、C型に分けられる。
②ウイルス表面の”HA”,”NA”の組み合わせで亜型が決まる。
③亜型によって感染する動物が異なる。
ウイルスに含まれるM1タンパクとNPタンパクによってA型、B型、C型に分けられます。
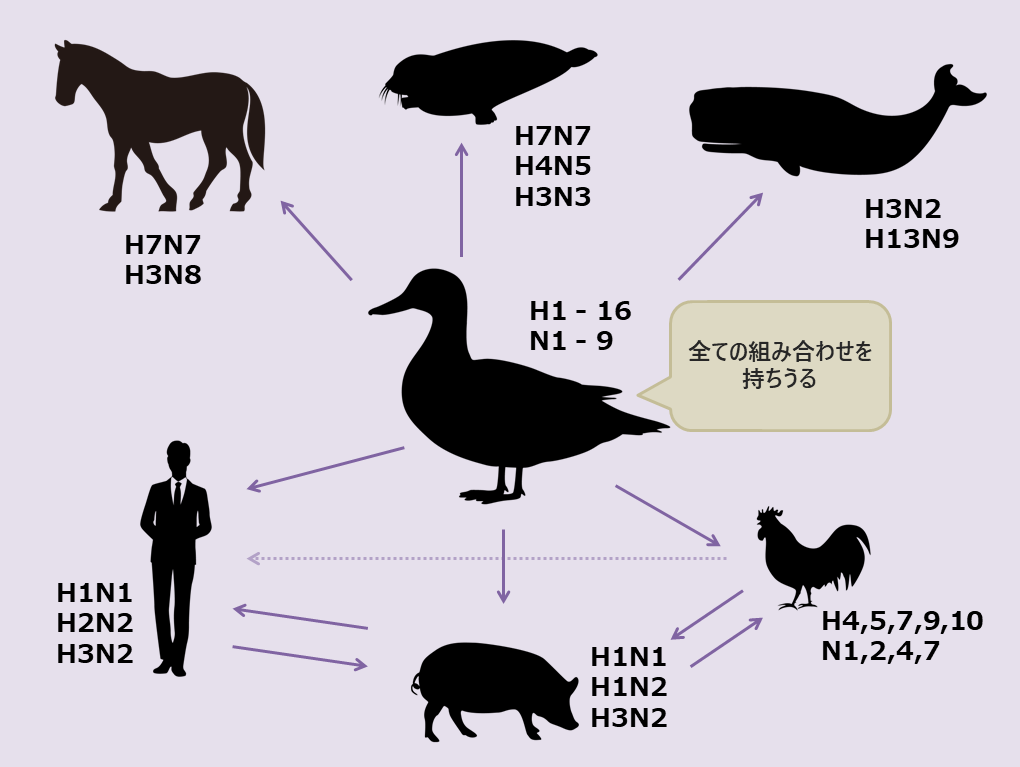
B型は人とアザラシ、C型は人とブタにだけ感染し、A型は様々な動物に感染します。
A型には、HAが16種類、NAが9種類あるので、16×9で144種類の亜型が存在する可能性があります。
B型にはNAとHAがそれぞれ1種類しかいないため亜型は無いとされており、C型にはそもそもNAが無く、亜型もありません。
インフルエンザウイルスには宿主特異性があります。
ウイルスのHAが宿主細胞の表面にあるレセプターに結合することで感染が始まるのですが、このレセプターが動物種ごとに異なるためです。
動物ごとに感染する亜型は決まっており、それは以下の図の通りです。
自然界では種を超えてインフルエンザが伝播することはまれなのですが、私たちは動物を家畜化することで”人ー動物”、”動物ー動物”の距離を短くしてしまいました。
これにより感染が広がりやすくなったほか、「遺伝子再集合」(後述)などの問題が生じています。
特に、「A型H1N1」は鳥、豚、人に感染しうるので大変危険です。
ニワトリから人には感染しないはずが…
人とニワトリではレセプターが異なります。
なので鳥インフルエンザは普通はニワトリから人に直接感染はしません。
しかし、人の肺の奥にニワトリと同じレセプターを持つ細胞が見つかりました。
つまり、ニワトリと濃厚接触することで、鳥インフルエンザは人に感染する可能性があります。
実際に2004年にベトナムでH5N1の鳥インフルエンザが発生した際は人に感染しました。
他にもアジアの他の国や中東でニワトリから人への感染が確認されています。
水鳥はウイルスの運び屋

「ウイルスの特徴と感染する動物」の図からも分かるようにカモなどの水鳥は全ての亜型に感染する可能性があります。
水鳥の中には長距離移動するものもいるので、インフルエンザは水鳥によって全世界に運ばれています。
鳥の体内ではウイルスは腸管で増えるため、ウイルスは糞と共に排出されます。
それが飼育されているニワトリなどの鳥に感染して、流行していきます。
2014年には南極のアデリーペンギンから新型が見つかったそうです。
これからウイルスが全地球に存在することが容易に想像できます。
このように水鳥はインフルエンザウイルスの「運び屋」なのです。
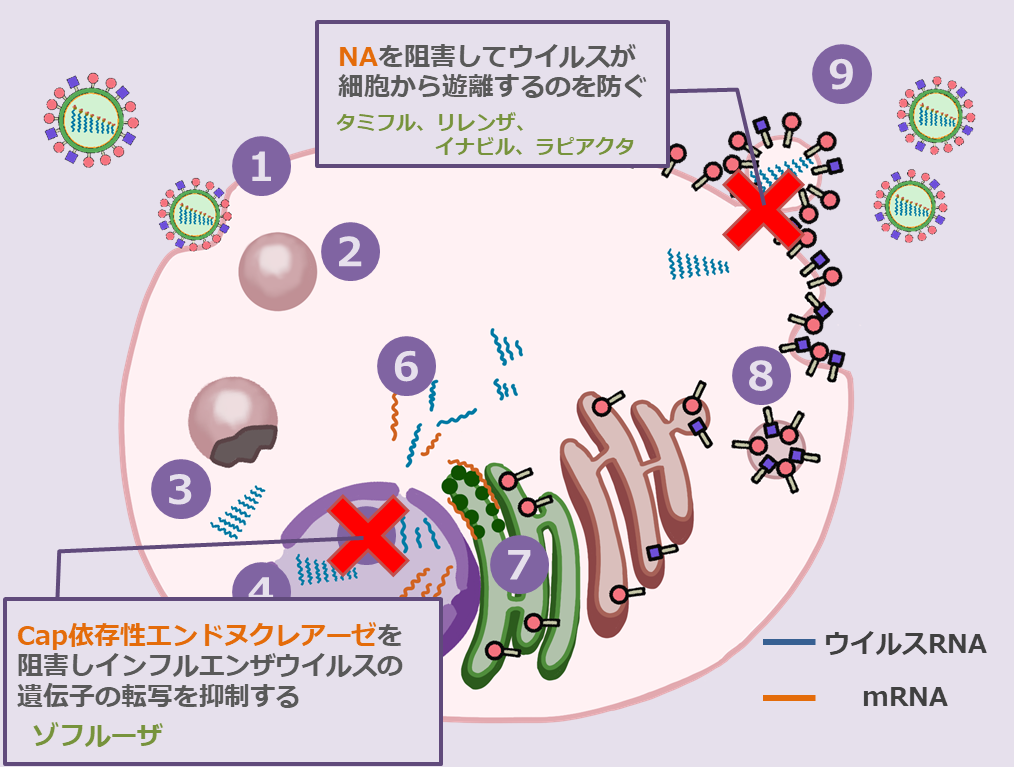
インフルエンザウイルスの増殖過程
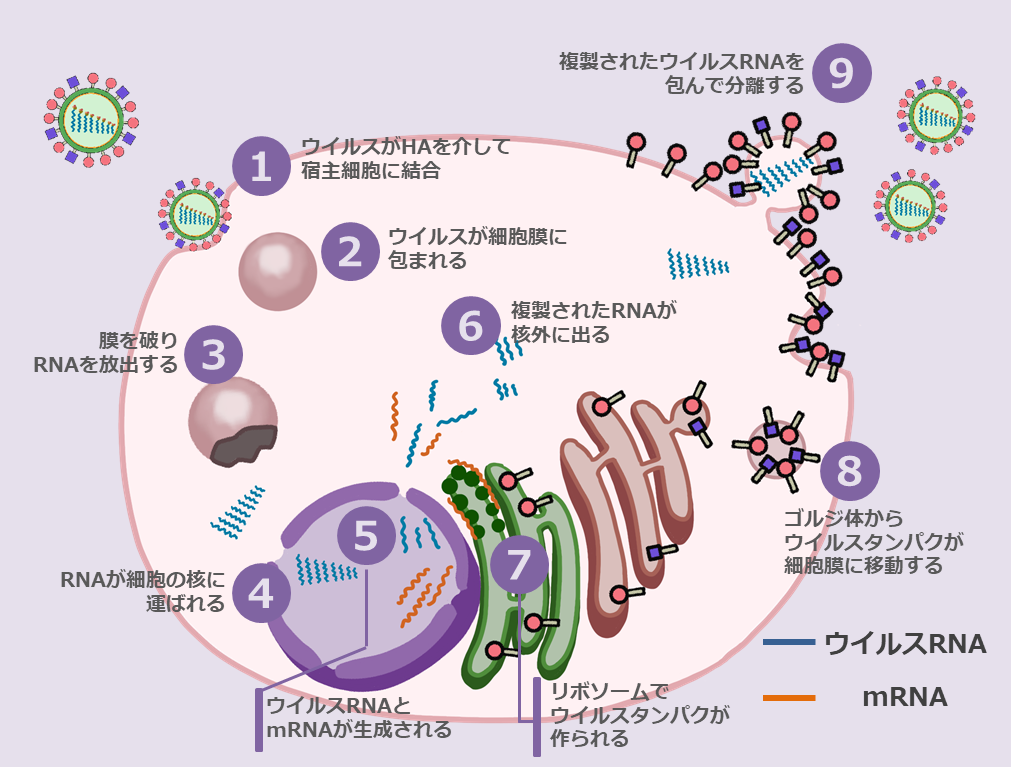
①ウイルス表面の「ヘマグルチニン(HA)」と細胞表面の「レセプター」が結合する。
②細胞はウイルスを細胞膜で包み込みながら内部に取り込む。
③M2タンパクの作用で膜を破り、細胞内にRNAを放出する(脱殻)。
④RNAは細胞の核に運ばれる。
⑤感染細胞の核内でウイルスRNAとmRNAが複製される。
⑥核内で複製されたウイルスRNAとmRNAが核の外に出る。
⑦mRNAは小胞体上のリボソームへと運ばれ、HAやNAといったウイルスのタンパク質が作られる。
⑧ゴルジ体から細胞質に出されたウイルスタンパクは細胞膜上に移動する。
⑨細胞膜が⑤で複製されたウイルスRNAをくるんで、宿主細胞から分離する。
外に出た新しいウイルスの表面には感染した細胞の細胞膜が少しついているのでNAがこれを取り除く働きを担っているそうです。
この仕組みでインフルエンザウイルスは1日に数十万倍に増殖すると言われています。
上の画像ではRNAの動きが分かりにくいので、RNAだけに焦点を当てた図を下に用意しました。
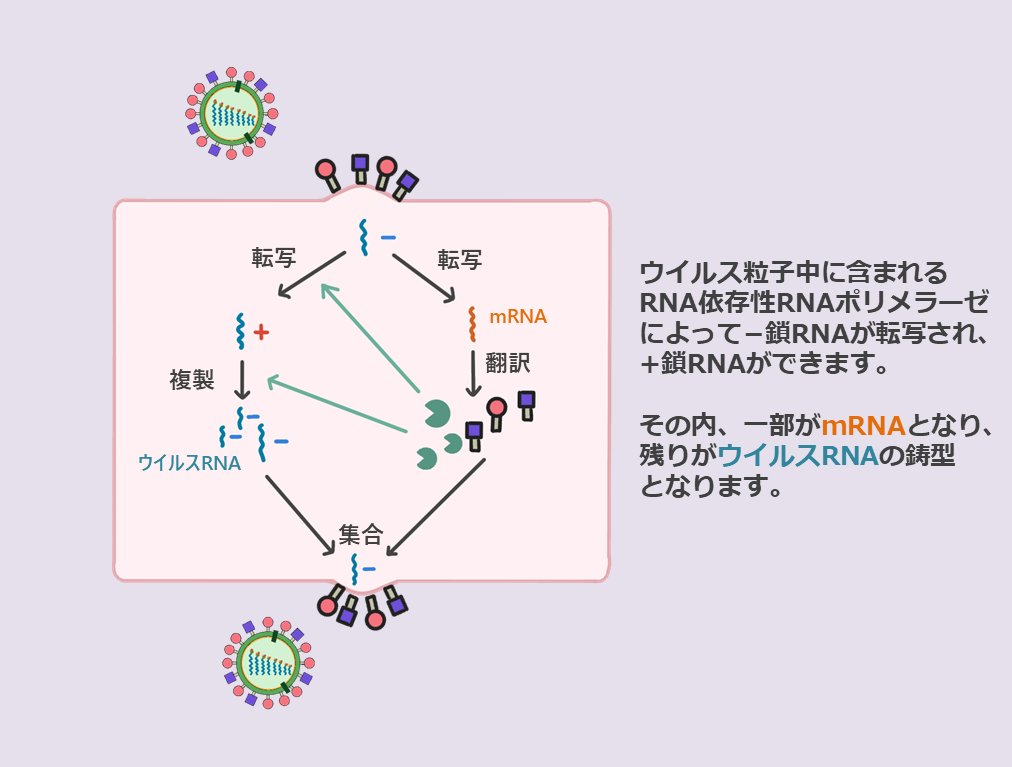
上にも書いたようにインフルエンザウイルスは1本鎖のマイナス鎖RNAに遺伝情報を保存しています。
これが細胞内に入ると、ウイルス粒子中にあって一緒に細胞内に侵入してきたRNA依存性RNAポリメラーゼによって−鎖RNAが転写され、+鎖RNAが作られます。
このうち一部がmRNA(オレンジ色)となり、ウイルスのタンパク質を作る設計図となります。
mRNAは翻訳されて、酵素やHA、NAなどのウイルス粒子を構成するタンパク質が作られます。
残りの+鎖RNAを元にしてウイルスRNAが複製されます。
これは元々ウイルス中に含まれていたRNAと同一のものです。
転写と複製は宿主細胞の核内で行われます。
最終的にタンパク質とウイルスRNAが集合して新たなウイルスが作られます。
”遺伝子再集合”で変異する
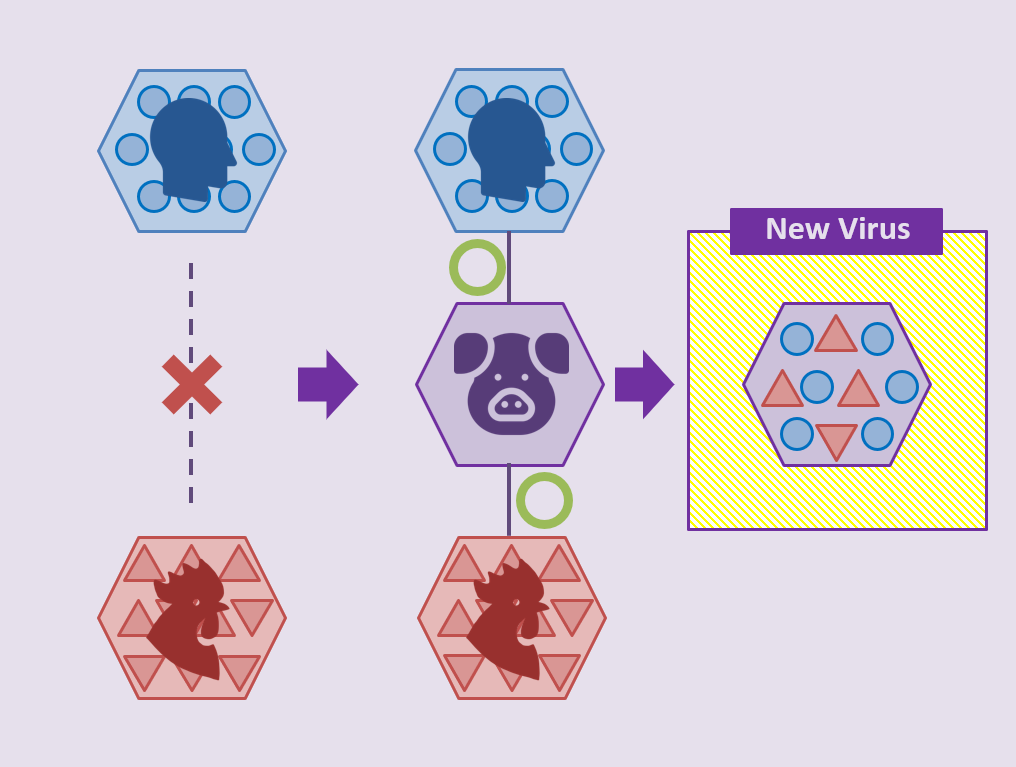
インフルエンザウイルスは2つの異なった株が同時に感染した細胞内では遺伝子再集合という現象が起こり、新たなウイルスが誕生します。
例えば豚の細胞には、人のウイルスも鳥のウイルスも感染できるのですが、感染が起こると2種類のウイルスの設計図であるRNAが豚の細胞内で混ざり合い新たなウイルスが誕生します。
1968年の香港型インフルエンザは、鳥のウイルスと人のウイルスが豚の呼吸器の細胞で再集合し、出現しました。
2009年にメキシコで発生した新型インフルエンザもこれによって生じたと考えられています
また、遺伝子再集合に加えてウイルスRNAが複製される過程で変異が起きやすく、新たなものが誕生することもあります。
DNAは2重らせん構造をとりますが、RNAは多くの場合1本鎖で存在するため、RNAの方が不安定で変異が起きやすいと言われています。
インフルエンザはとても多様性に富むウイルスなので、「人類に最後まで残る感染症」と言われているそうです。
新型インフルエンザの脅威
「インフルエンザが変異しやすいことは分かったけど、毎年流行ってるあれは何なの?」
「インフルエンザは毎年のように流行ってるじゃん。全然危険じゃないでしょ。」
と考えている人がいると思います。
毎年流行しているインフルエンザは「季節性インフルエンザ」と呼ばれています。
これは以前流行したものが少しだけ変異して誕生したものです。
つまり、多くの人が免疫を持っているのです。
一方で、新型インフルエンザは違います。
これは今までに流行したことのない、もしくはかなり前に流行した亜型のウイルスによります。
なのでほとんどの人が免疫を持っておらず、流行が急速に拡大する恐れがあります。
スペイン風邪のインフルエンザウイルスは、H1N1鳥インフルエンザと比べてRNAポリメラーゼ遺伝子に10箇所の変異がありました。
H5N1鳥インフルエンザウイルスでも、この内の3箇所にすでに変異が起きているそうです。
つまり、H5N1鳥インフルエンザウイルスがスペイン風邪を引き起こしたウイルスのように、毒性の高い新型インフルエンザウイルスに変化しつつあるということです。
実験で人為的にH5N1の遺伝子をさらに変化させると、フェレットに感染しやすくなり、飛沫感染を引き起こしたそうです。
スペイン風邪のようなパンデミックが起こるのも時間の問題かもしれません。
WHOによると新型インフルエンザが世界で流行した場合、200~5000万人もの人が死亡すると予想されています。
感染経路
感染経路は2通りあります。
「飛沫感染」
感染者のくしゃみや咳の飛沫とともにウイルスが放出され、それを他の人が吸い込むことで感染。
「接触感染」
感染者が咳などを手で押さえ、その手でどこかに触り、別の人が同じところに触れてウイルスが手に付着し、その手で口や鼻を触り粘膜から感染。
予防法
・正しい手洗い
・健康管理
・予防接種
・適度な湿度を保つ
・人混みへ行かない
予防としては手洗いが一番有効なようです。
石鹸を付けて”正しく”、”こまめに”行うようにしましょう。
予防接種を受けてもインフルエンザにかかることはありますが、重症化を防ぐことが期待されるので、ご高齢の方や、妊婦、持病のある方など、重症化しやすい人は打っておくと良いと思います。
また、マスクを着用することで咳をした際に飛散したウイルスを吸い込むのを防ぎますし、感染者が付けることでウイルスが飛び散るのを防ぐ働きがあります。
治療法
・オセルタミビル(タミフル) 経口薬
・ザナミビル(リレンザ) 吸入薬
・ラニナミビル(イナビル) 吸入薬
・ペラミビル(ラピアクタ) 注射薬
つい最近までインフルエンザの治療薬は、上の4種類でした。※()内は商品名
これらは全てノイラミニダーゼ(NA)阻害薬で、ウイルスが感染細胞から遊離するのを防いでいます。
2018年に新しい抗インフルエンザ薬の「バロキサビル・マルボキシル(ゾフルーザ)」が登場しました。
この薬はCap依存性エンドヌクレアーゼを阻害し、インフルエンザウイルスの遺伝子の転写を抑制するという、上の4つの薬とは作用機序が異なるものです。
また、1回の服用で治療が完了します。
まだ新しい薬であるため、以前の「ノイラミニダーゼ阻害薬」とどのように使い分けされるべきであるかは明らかではありませんが、重症者に対しては両者を併用したり、この薬はウイルスの排出期間を短くする特徴があるので感染を早急に防ぎたい状況(院内感染や高齢者施設での流行)ではゾフルーザを使用したほうが望ましいと考えられています。
Cap依存性エンドヌクレアーゼ
宿主(感染された個体)のmRNAの末端には「Cap構造」があり、mRNAを安定させる働きがあります。
ウイルスのポリメラーゼは「PA」、「PB1」、「PB2」の3つのサブユニットからなります。
はじめに、PB2が宿主細胞のmRNAのCap部分を捕まえます。
次に、PAが宿主の遺伝子部分を切り取りるのですが、この時に使われる酵素が「Cap依存性エンドヌクレアーゼ」です。
その後、PB1がウイルスの遺伝子を差し替えます。
この一連の流れは「キャップスナッチング」と呼ばれます。
パンデミックの歴史
スペイン風邪(1918年)

H1N1亜型のインフルエンザウイルスが原因。
当時の世界人口16億人の内、5億人もの人が感染したと言われています。
全世界で2000~4000万人もの死者が出ました。
これは第一次世界大戦の死者1000万人を大きく上回る数字です。
スペインという名前がついていますが、流行はアメリカで始まりました。
第一次世界大戦中であったため、アメリカから多くの兵士がヨーロッパに移動し、それに伴いウイルスもヨーロッパをはじめ、世界中に広がっていきました。
戦争中に自国でインフルエンザが流行っていることを敵に知られたくなかったので、多くの国が自国で流行していることを隠していました。
しかし、スペインは参戦していなかったためインフルエンザの流行を公表し、それが由来で「スペイン風邪」と呼ばれています。
日本では1918年10月から流行が始まりました。
患者は多い時で2,100万人にものぼり、当時の日本の人口は5,600万人だったので、全国民の37.5%が罹患していたことになります。
流行は1919年、1920年と3年間も続きこの間におよそ40万人が亡くなりました。
アジア風邪(1957年)

H2N2亜型が原因。
1957年に香港で発見されたとされていますが、ほぼ同じ時期にシンガポール、台湾、マニラでも見つかっています。
世界でおよそ200万人が亡くなりました(調査した期間によって死亡者数は100~400万人もの開きがあります)。
日本でも同年の5月に発生しました。季節性のインフルエンザがちょうど収まったころだったそうです。
5月の上旬に発見され、下旬にはほぼ全国に広がりました。
日本では65~300万人がかかり、5,700人が死亡しました。
この流行は夏にいったん収まりますが、秋になると再び流行し、春まで流行していました。
夏に流行が下火となったのは、学校が夏休みに入ったことと、仕事場でも今みたいにクーラーなどはあまり使われていなかった時代だったので、窓を開けて常に換気していたためだと考えられています。
アジアインフルエンザは重度な臨床症状は示さなかったようで、季節性インフルエンザと大差なかったそうです。
スペイン風邪が流行した際は合併症で細菌性肺炎を発症する人が多く、それが死亡率の高さの主な原因でした。
しかしアジア風邪の時には抗生物質が普及していたのでこれが死亡率の減少に大きく貢献したと考えられています。
(細菌だけでなくウイルス自体も肺炎を引き起こしうる考えられています)
香港風邪(1968年)

H2N2亜型が原因。
1968年6月に香港で流行が始まりました。7月末に日本、8月にはシンガポール・台湾、9月にはマニラ・バンコク・インド・ヨーロッパ・ロシアに広がっていきました。
当時はベトナム戦争の最中で、帰還した兵士によってアメリカにも到達したとされています。
多くの地域に広がりましたが、スペイン風邪・アジア風邪と比べると被害はとても小さく終わりました。
しかし、この香港インフルエンザはその後季節性インフルエンザとして流行し、遺伝子の変異を繰り返しながら半世紀にわたって人類を苦しめています。
国内でも大流行はありませんでしたが、季節性インフルエンザとなったあとは流行が見られています。
ソ連風邪(1977年)
H1N1亜型が原因。
1977年5月に中国北西部から始まり、12月までにシベリア、西部ロシアに広がっていきました。
日本にも12月には到達しており、翌年の6月までにアメリカ、ヨーロッパ、南米に広がっていきました。
しかしこの亜型は、50年代に流行した「イタリア風邪」と遺伝子的に同一であったため、23歳以上の人は抗体を持っておりほとんど感染せず、免疫を持たない23歳未満の人を中心に感染が広がりました。
それ以来25年続き、少しづつ変異しているそうです。
新型インフルエンザ(2009年)

2009年4月24日にWHOから豚由来の新型インフルエンザ(H1N1亜型)がメキシコで発生したとの報告がありました。
これはメキシコにおいて、人のインフルエンザと鳥インフルエンザが豚の体内で混ざり合って誕生したものだと考えられています。
感染は広がり、6月12日にはWHOが警戒レベルを最高のフェーズ6に引き上げることになります。
流行初期にメキシコで高い死亡率を示すと報道されていましたが、実際はそこまで高くはありませんでした。
1年4か月後の2010年8月10日に警戒レベルが下げられました。
214の国と地域で7億人から14億人もの人が感染し、およそ1万8千人の死者が出たとされています。
鳥インフルエンザとは?
鳥インフルエンザについては他の記事で紹介したいと思います!
インフルエンザと聞くと季節性のものが身近であるのであまり危険だと感じませんよね。
ですが実際は多くの動物に感染し、とても変化に富むウイルスなのです。
人類が全く免疫を持たない新型インフルエンザが出るのは時間の問題だと考えられています。
その時は、今回のコロナで得た教訓を活かしていけるのではないでしょうか。
最後まで読んでいただきありがとうございました!
参考
https://www.gov-online.go.jp/useful/article/200909/6.html#section3
http://medical.radionikkei.jp/kansenshotoday_pdf/kansenshotoday-190206.pdf
https://www.cas.go.jp/jp/influenza/kako_10.html
https://www.bloomberg.co.jp/news/articles/2009-05-12/KJIF2D0D9L3501
http://www.tokyo-eiken.go.jp/sage/sage2005/
https://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou04/dl/infu100528-02.pdf
https://www.jstage.jst.go.jp/article/naika/102/10/102_2705/_pdf
・「感染症のはなし 新興・再興感染症と闘う」 中島秀喜 朝倉書店 2012年
・「ウイルスと感染症 エボラ出血熱、デング熱、新型インフルエンザ 世界を震撼させるパンデミック」 ニュートンプレス 2015年
・「獣医微生物学 第3版」 見上彪 文永堂出版 2016年